 |
국내 화장품 기업들은 현실적 어려움에 부딪혀 중국 및 동남아 진출에 집중하고 있지만 가까운 미래에는 유럽 시장을 공략하는 기업이 늘어날 것으로 예상된다.
특히 EU 차원의 통합 규정이 올해 7월부터 발효되면 행정적 판매절차가 간소화 되는 것이 유럽 화장품 시장 진출에 큰 영향을 끼칠 전망이다.
우선 EU 차원의 단일 신고 제도가 도입된다. 지금까지 화장품 제조 또는 판매업체는 진출하려는 회원국마다 신고 절차를 거쳐야 했지만 통합 규정이 발효되면 EU 집행위에 ▲상품명 ▲제품 카테고리 ▲책임자 명과 주소 ▲원산지 국가 ▲출시 회원국명 ▲나노 물질 함유 여부 ▲CAS 번호(CMR 물질 함유일 경우) ▲라벨 ▲포장 사진 등을 한번만 제출하면 된다.
제조규격도 ‘DIN EN ISO 22716’을 권장하고 있어 EU회원국은 자국 규격으로 이 국제표준규격보다 더 엄격한 규격을 요구할 수 없다.
유통 책임자는 EU 회원국 중 한 국가에 등록된 사업등록자로서 제품이 새 규정에 적합함을 보증해야 한다. 또한 제품 포장에 사업자명(업체명)과 주소를 표기해야 한다. 유통 책임자 지명 시 전문성이 규정 상 요구되는 것은 아니나 제품에 대한 지식을 충분히 소유하고 있어야 한다.
이는 불량 제품 발생 시 제품을 분석・평가해 시장 철수와 리콜을 포함한 규정이 정한 모든 조치를 취해야 하기 때문이다. 또한 유통 책임자는 당국이 요구할 때 즉시 제출할 수 있도록 제품에 대한 모든 정보 및 서류와 소매상을 포함해 모든 유통 체인에 연계된 업자 리스트를 보관하고 있어야 한다.
적합성 평가에 대한 기준도 변경된다. 제품의 안전성 및 적합성 평가는 학위나 특수 연수, 경력에 의한 자격을 가진 사람이 평가해야 하고 샘플분석 방법은 믿을 수 있고 재생산 할 수 있으며 시장에 나 와 있는 최신 방법을 사용해야 한다. 다만 표준 규격은 아직 마련되지 않은 상태다. 현재 유럽에서는 독일 화장품 과학연구소 및 독일 화장품 산업협회의 인증과 자격 연수 과정이 높은 신뢰를 받고 있다.
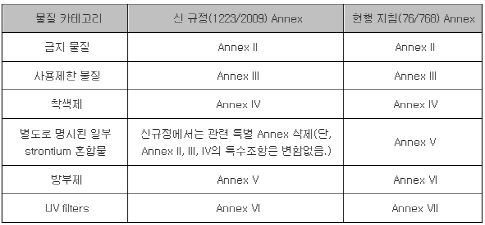
사용금지·제한·착색제·방부제·자외선차단 물질과 관련한 지침은 지금과 크게 바뀌지 않는다. 다만 물질 카테고리가 명기된 Annex 번호는 일부 변경됐다. 또한 안전성 평가 보고서를 제출 시 기술적으로 사용금지물질을 함유하지 않았음을 입증해야 한다.
사용금지·제한·착색제·방부제·자외선차단 물질 관련 현행 지침과 신규정 비교
 |
최종 제조법이나 성분 또는 복합성분이 동물 실험된 화장품은 EU에서 판매할 수 없으며 반복적으로 사용되는 물질의 독성 또는 물질이 생식에 미치는 영향과 독성 발생에 대한 연구를 위한 동물실험은 예외적으로 2013년 3월 11일까지만 허용하고 있다.
소비자에게 제품관련 정보를 제공하기 위한 라벨표시 사항도 명시됐다. 라벨은 제품이 판매될 각 국가의 언어로 ▲제품 책임자 명 또는 업체명 및 주소 ▲원산지 국명 ▲내용물의 중량 또는 부피 ▲제품의 사용 유효기간 ▲사용주의 사항(전문가용 제품 포함) ▲제품 제조번호 ▲성분리스트 등을 명기해야 한다.
Copyright ⓒ Since 2012 COS'IN. All Right Reserved.