# 생체활성분자 고효율 전달 위한 광활성 콜라겐 하이드로젤 나노소재
자극 반응성 나노입자는 높은 안정성과 방출 제어 성능을 지녀 생체활성분자의 효과적인 세포 내 전달을 위한 나노 운반체로 많은 관심을 받고 있다. 이 연구는 치료 단백질의 세포 내 전달을 위한 빛 또는 열 반응성 금-콜라겐 하이드로젤 나노입자(Au-CHP)를 개발하고 이를 응용하는 데에 초점을 맞추고 있다.
빛 자극에 노출되면 Au-CHP는 금 나노입자의 광열 전환 특성을 통해 빠르게 국부 온도를 상승시키며 이를 통한 콜라겐 하이드로젤의 구조 변형으로 단백질의 안전한 방출과 빠른 확산을 유도해 세포 증식도 향상, 활성 산소종 제거와 3차원 세포배양체 성장을 촉진한다는 것을 관찰했다. 더욱이 Au-CHP는 금 나노입자의 밀도 조절을 통해 광열 전환에 의한 발열을 미세 조정해 단백질과 같은 열 민감성 약물의 활성을 유지한 채 세포 내로 전달이 용이했다.
단백질은 효소 촉매작용, 유전자 발현, 세포 분열과 자멸의 조절 등 생물학적 과정에서 중요한 역할을 담당한다. 그러나 돌연변이와 이에 따른 비정상적인 기능으로 인해 심각한 질병이 발생하곤 한다. 이를 해결하기 위해서 최근 수십 년 동안 성장인자(growth factor), 단일클론 항체(monoclonal antibody), 사이토카인(cytokine) 등을 이용해 질병을 치료하는 분자 수준의 단백질 치료제가 개발돼 왔다. 이는 생체 유래 약물로 분류돼 부정적인 부작용과 면역 반응을 일으킬 가능성이 적기 때문에 분자 수준 치료에서 강력한 수단으로 여겨졌다.
그러나 단백질 치료제는 외부 자극으로 인한 변성 또는 프로테아제에 의한 분해로 인해 세포 전달 과정에서 구조가 손상될 가능성이 매우 높다. 이를 해결하고자 단백질을 세포에 직접 전달하기 위해 미세주입법(microinjection), 전기천공법(electroporation)과 세포 투과 펩타이드(cell penetrating peptide) 접합 등 여러 물리화학적 방법이 사용됐다.
Au-CHP의 합성 방법과 물리화학적 특성
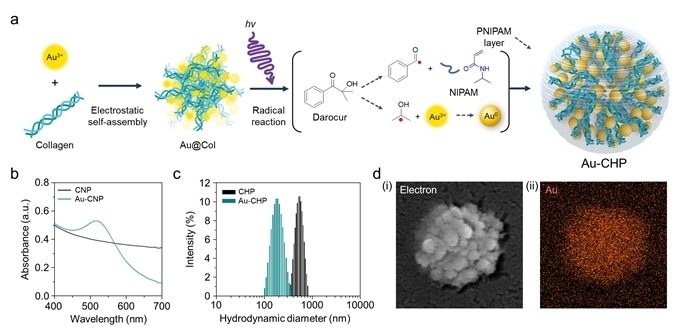
이 중 세포 투과 펩타이드는 30개 미만의 아미노산으로 구성된 세포 침투능이 매우 높은 펩타이드 서열로 질병 진단과 치료를 위한 전임상 연구들에 높은 빈도로 광범위하게 사용된다. 그러나 펩타이드 구조 역시 단백질과 동일하게 안정성이 상대적으로 좋지 않아 전달 조건에서 분해돼 기능을 잃을 수 있다.
앞서 언급한 치료용 단백질 또는 펩타이드 서열의 변성과 분해를 최소화하기 위해서는 일반적으로 안전하게 보호돼 목표 부위까지 도달할 수 있는 전달체의 존재가 필수적이며 이 중 가장 대중적으로 사용되는 소재는 고분자 소재인 하이드로젤(hydrogel)이다. 하이드로젤은 수용액 상에서 높은 담지 효율과 손쉬운 구조 변형을 통해 단백질과 같은 거대분자도 캡슐화할 수 있기 때문에 활용도가 매우 높다.
하이드로젤 내부의 네트워크 구조는 우수한 친수성을 가진 고분자 사슬을 기반으로 하며 외부 변화에 민감하게 반응하는 기능기를 추가해 자극 감응성 전달체로도 사용할 수 있다. 예를 들어 pH, 산화환원(redox)과 온도 변화는 내부 담지된 약물 방출을 위한 자극원으로 많이 선택돼 왔다. 그러나 이러한 자극들은 대체로 약물 구조의 손상을 야기할 수 있으며 침습성이 낮아 생체 내 방출 제어가 용이하지 않다.

Copyright ⓒ Since 2012 COS'IN. All Right Reserved.
#코스인 #코스인코리아닷컴 #코스메틱저널코리아(CJK) #화장품 #코스메틱 #2024년5월호 #화장품연구개발마케팅전문저널 #최신연구 #기술정보 #생체활성분자 #콜라겐 #하이드로젤 #Au-CHP #단일클론항체 #사이토카인 #프로테아제 #미세주입법 #전기천공법 #아미노산 #펩타이드 #산화환원 #초음파 #광열전환 #NIPAM #서울시립대학교 #최인희교수 #하이드록시프롤린 #벤조페논 #아마이드 #과산화수소